|
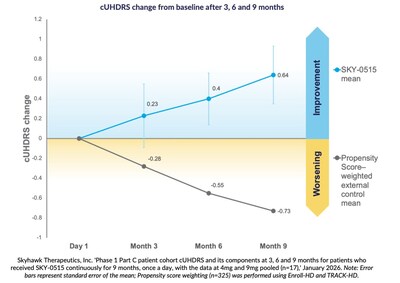
Penemuan sembilan bulan menunjukkan peningkatan purata pada Skala Penilaian Penyakit Huntington Bersatu Komposit (cUHDRS) sebanyak +0.64 mata daripada garis asas, berbanding dengan jangkaan kemerosotan cUHDRS berdasarkan sejarah semula jadi pada pesakit simptomatik sebanyak -0.73 mata dalam tempoh sembilan bulan, berdasarkan pemberat skor kecenderungan.
Skyhawk juga mengumumkan bahawa ujian Fasa 2/3 FALCON-HD bagi SKY-0515 telah diperluaskan ke peringkat global. Skyhawk kini telah memberi dos kepada lebih 90 pesakit.
BOSTON, 29 Januari 2026 /PRNewswire/ — Skyhawk Therapeutics, Inc., sebuah syarikat bioteknologi peringkat klinikal yang membangunkan terapi molekul kecil baharu untuk memodulasi sasaran RNA kritikal, hari ini mengumumkan keputusan positif daripada analisis interim sembilan bulan bagi rawatan penyiasatan syarikat terhadap penyakit Huntington (HD) dengan SKY-0515.
Rawatan dengan SKY-0515 menunjukkan pengurangan bergantung dos bagi protein mHTT dalam darah sebanyak 62% pada dos 9mg, serta pengurangan mRNA PMS1 bergantung dos sebanyak 26%. PMS1 merupakan pemacu utama bagi pengembangan ulangan CAG somatik dan patologi penyakit Huntington. SKY-0515 juga telah menunjukkan pendedahan sistem saraf pusat yang sangat baik serta umumnya selamat dan boleh diterima dengan baik.
Pada tiga, enam, dan sembilan bulan, pesakit yang menerima SKY-0515 dalam kohort pesakit Bahagian C ujian klinikal Fasa 1 menunjukkan peningkatan purata pada Skala Penilaian Penyakit Huntington Bersatu Komposit (cUHDRS) berbanding garis asas. Pada sembilan bulan, dalam analisis terkumpul, peningkatan ini ialah +0.64 mata berbanding kemerosotan cUHDRS yang dijangka sebanyak -0.73 mata pada pesakit simptomatik, berdasarkan pemberat skor kecenderungan menggunakan data Enroll-HD dan TRACK-HD.
"Saya sangat digalakkan dengan data keselamatan dan keberkesanan awal daripada ujian Fasa 1 Bahagian C SKY-0515 pada pesakit, yang menunjukkan penyimpangan dalam cUHDRS daripada kemerosotan sejarah semula jadi yang dijangka pada analisis yang telah ditetapkan pada tiga, enam, dan sembilan bulan," kata Ed Wild, Profesor Neurologi di University College London. "SKY-0515 terus mengurangkan protein mHTT pada tahap tertinggi yang pernah ditunjukkan oleh mana-mana terapi yang diuji setakat ini pada pesakit, dengan data klinikal dan biomarker menunjukkan ubat ini boleh diterima dengan baik pada semua dos yang diuji. Keupayaan SKY-0515 untuk mengurangkan kedua-dua mHTT dan PMS1 menawarkan gabungan berkuasa untuk merawat penyakit Huntington melalui dua mekanisme patogen utama penyakit ini. Keputusan ujian terbuka ini, yang akan disahkan dalam ujian kawalan plasebo FALCON-HD yang sedang dijalankan, memberikan jangkaan impak bermakna bagi pesakit HD di seluruh dunia – bagi mereka, rawatan penurunan huntingtin secara oral seperti SKY-0515 akan benar-benar transformasi."
"Matlamat kami bagi kajian Fasa 1 adalah untuk menilai keselamatan dan aktiviti biomarker," kata Sergey Paushkin, Ketua R&D di Skyhawk Therapeutics, "dan kekuatan berterusan tindak balas biomarker SKY-0515 dalam analisis data interim sembilan bulan – serta peningkatan pada penanda hasil berpotensi, cUHDRS, berbanding kemerosotan skor cUHDRS dalam data sejarah semula jadi pesakit – menekankan potensi SKY-0515 sebagai terapi pengubah penyakit kelas terbaik bagi HD. Data interim ini merupakan pencapaian penting bagi SKY-0515 dan menyerlahkan keupayaan platform Skyhawk untuk menghasilkan molekul kecil pertama seumpamanya bagi penyakit serius yang tiada terapi pengubah penyakit yang diluluskan."
Penyakit Huntington ialah gangguan neurodegeneratif jarang, diwarisi, dan akhirnya membawa maut yang menjejaskan lebih 40,000 pesakit simptomatik di Amerika Syarikat, dengan ratusan ribu dianggarkan terjejas di seluruh dunia. Pada masa ini, tiada rawatan diluluskan yang mampu memperlahankan atau menghentikan perkembangan penyakit. SKY-0515 ialah molekul kecil modulator RNA yang diberi secara oral dan sedang disiasat, dibangunkan melalui platform modulator RNA baharu syarikat, SKYSTAR®. SKY-0515 secara terapeutik mengurangkan kedua-dua protein HTT dan protein PMS1. PMS1 merupakan pemacu tambahan utama bagi pengembangan ulangan CAG somatik dan patologi HD, serta dijangka melengkapi manfaat pengurangan mutant HTT.
Skyhawk juga mengumumkan hari ini bahawa ujian Fasa 2/3 FALCON-HD SKY-0515, yang dibuka di dua belas lokasi di Australia dan New Zealand, telah diperluaskan ke peringkat global. Skyhawk kini telah memberi dos SKY-0515 kepada lebih 90 pesakit.
SKY-0515 merupakan ubat pertama Skyhawk dalam ujian klinikal.
Skyhawk menjangkakan akan membawa masuk ubat molekul kecil tambahan untuk merawat penyakit neurologi jarang yang tiada terapi pengubah penyakit diluluskan ke dalam klinik menjelang akhir 2027.
Maklumat tentang Kajian Klinikal Fasa 1 SKY-0515
Ujian klinikal Fasa 1 SKY-0515 ialah ujian manusia pertama yang direka untuk menilai keselamatan, toleransi, farmakokinetik dan farmakodinamik SKY-0515 pada sukarelawan sihat dan individu dengan penyakit Huntington (HD) peringkat awal. Ujian ini dibahagikan kepada tiga bahagian. Bahagian A dan B menilai SKY-0515 pada Sukarelawan Sihat. Bahagian C ialah kajian reka bentuk selari kawalan plasebo buta dua peringkat bagi dua tahap dos SKY-0515 dan plasebo pada individu dengan HD peringkat awal (HD-ISS Tahap 1, 2, atau Tahap 3 ringan) selama 84 hari, diikuti sambungan rawatan aktif selama 12 bulan di mana semua peserta akan menerima sama ada dos rendah atau tinggi SKY-0515 secara buta. Objektif kajian termasuk menilai protein mutant HTT dan mRNA PMS1. Pesakit pertama telah menerima dos dalam Bahagian C SKY-0515 pada Januari 2025. Pendaftaran bagi Fasa 1C ujian SKY-0515 kini telah lengkap.
Maklumat tentang Kajian Klinikal Fasa 2/3 FALCON-HD SKY-0515
FALCON-HD (NCT06873334) ialah kajian rawak Fasa 2/3, buta dua, kawalan plasebo, julat dos, untuk menilai farmakodinamik, keselamatan, dan keberkesanan SKY-0515 pada 120 peserta dengan HD Tahap 2 dan awal Tahap 3 di 12 lokasi di Australia dan New Zealand, serta 400 peserta dengan HD Tahap 2 dan awal Tahap 3 di lebih 40 lokasi di seluruh dunia. Pesakit yang layak akan menerima satu dos oral SKY-0515 sekali sehari pada salah satu daripada tiga tahap dos atau plasebo, untuk tempoh rawatan sekurang-kurangnya 12 bulan. Ujian ini bertujuan menilai potensi SKY-0515 untuk memodulasi pemisahan RNA dan mengurangkan protein mHTT dan PMS1, yang terlibat dalam patologi penyakit Huntington. Maklumat tambahan tentang FALCON-HD, termasuk lokasi penyertaan dan kriteria kelayakan, boleh diperoleh di ClinicalTrials.gov dan www.FALCON-HD.com.
Maklumat tentang Skyhawk Therapeutics
Skyhawk Therapeutics ialah sebuah syarikat bioteknologi peringkat klinikal yang menggunakan platform proprietarinya, SKYSTAR®, untuk menemui dan membangunkan terapi pemodulasi RNA bermolekul kecil bagi merawat penyakit paling sukar ditangani di dunia. Untuk maklumat lanjut sila layari www.skyhawktx.com.
Pihak Hubungan Skyhawk
Maura McCarthy
Ketua Pembangunan Korporat
[email protected]
Gambar – https://mma.prnewswire.com/media/2870056/Skyhawk_Therapeutics_9_MONTH_DATA_Graph.jpg
Logo – https://mma.prnewswire.com/media/710814/Skyhawk_Therapeutics_Logo.jpg
Sumber artikel: http://www.prnasia.com/asia-story/archive/4871512_MS71512_6